|
Naturwissenschaften Chemie |
 |
Naturwissenschaften Weitere Informationen |
|
|
Radiochemischer
Nachweis von superschweren Elementen
|
 |
 |
|
Schwerelemente
mit den Ordnungszahlen 115 und 113
|
 |
Erstmals
war eine Schweizer Forschungsgruppe massgebend an der Entdeckung neuer
chemischer Elemente beteiligt.
 |
| Die
beiden Schwerelemente tragen die Ordnungszahlen 115 und 113, wie
Untersuchungen anhand von Zerfallsketten im russischen Kernforschungszentrums
Dubna belegten. Mit einem eleganten radiochemischen Nachweis steuerte das
Paul Scherrer Institut (PSI) wesentlich zum Erfolg bei.
Die
Chemie dringt weiter in wissenschaftlich unbekannte Gebiete vor. Bis 1940
galt Uran als das schwerste chemische Element. |
|
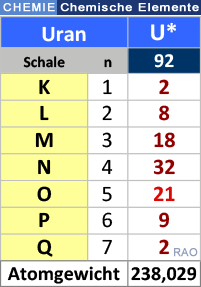
Das
in der Natur vorkommende Metall trägt die Ordnungszahl 92, sind doch
in seinem Atomkern 92 positiv geladene Protonen vorhanden. Seither sind
über 20 nur künstlich herstellbare Elemente mit höheren
Ordnungszahlen entdeckt worden. |
 |
Geburtsstunde
von Element 115
Schwere
Elemente zerfallen über Kaskaden von elektrisch geladenen Helium-Atomen,
so genannten Alphateilchen. Solche Zerfallsketten nutzten amerikanische,
russische und Schweizer Wissenschaftler, um die bisher nur theoretisch
angenommenen und noch namenlosen Elemente 115 und 113 experimentell nachzuweisen.
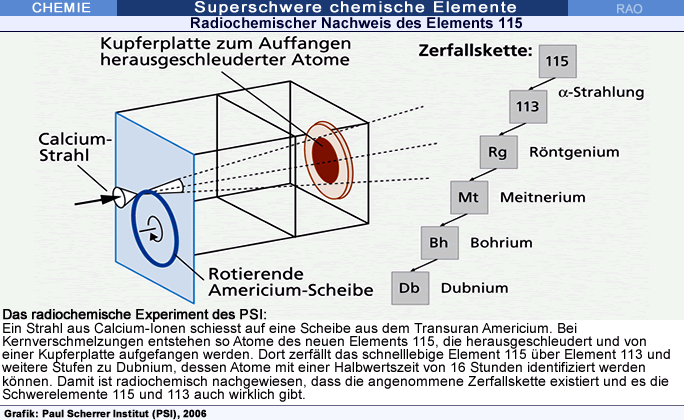
Zur Synthese von Atomen des Elements 115 bombardierten
die Forscher eine rotierende Scheibe aus Americium,
einem Transuran der Ordnungszahl 95, mit einem Calcium-Strahl.
nach
oben
 |
| Dabei
traten in seltenen Fällen Kernverschmelzungen auf: die Geburtsstunde
des neuen Elements 115. Damit war dessen Existenz aber noch nicht bewiesen. Seine
Atome leben nur kurze Zeit, etwa eine Zehntelssekunde,
und sind daher schwierig aufzuspüren. |
|
Während vorgängig
der physikalische Nachweis von Element-115-Atomen durch spezielle Detektoren
bloss drei Treffer ergab, verlief der radiochemische Pfad fünfmal
erfolgreicher.
Radiochemischer
Nachweis mit 15 Zerfallsatomen
Wie
erwähnt zerfällt Element 115 unter Aussendung eines Alphateilchens
zuerst zu Element 113 und dann über weitere Emissionen von Alphateilchen
(Helium-Kerne) zu Dubnium mit
der Ordnungszahl 105.
 |
| Hier
setzte der elegante experimentelle Beweis des PSI-Teams an:
Es
installierte hinter der rotierenden Americium-Scheibe
eine Kupferplatte, welche die herausgeschleuderten Element-115-Atome auffing.
Wenn darauf sich nach einer gewissen Zeit Dubnium-Atome (mit einer Halbwertszeit von 32 Stunden)
nachweisen lassen, wäre die Verifikation vollbracht. |
|
Tatsächlich
konnten die Forscher insgesamt 15 Dubnium-Atome identifizieren
und damit erfolgreich beweisen, dass die angenommene Zerfallskette auch
wirklich existiert. Der physikalische Nachweis liess sich so radiochemisch
untermauern.
«Die
Schweizer Wissenschaft konnte eine Premiere feiern - wenn auch im Ausland»,
bilanziert Heinz Gäggeler, Forschungsbereichsleiter am PSI und Chemieprofessor
an der Universität Bern, der die Schweizer Gruppe leitete. Beim Wettlauf
um die ständige Erweiterung des Periodensystems ist erstmals auch
die Schweiz vorne dabei. Die Versuche erforderten dazu
jedoch den Schwerionenbeschleuniger mit der weltweit höchsten Intensität
an Calcium-Strahlen. Diese Anlage steht im Kernforschungszentrum
Dubna, 120 Kilometer nördlich von Moskau. über 6000 Personen
arbeiten in dieser riesigen Forschungsstätte an den Ufern der Wolga.
nach
oben
 |
| Quelle:
Text Paul Scherrer Institut (PSI), 2006 |
nach
oben
 |
| Isotop
(gr: isos = gleich, topos: gleicher Ort)
Als
Isotope werden Atome bezeichnet, welche die gleiche Elektronen- und Protonenzahl
haben, sich aber in der Anzahl ihre Neutronen unterscheiden. Diese Atome
zeigen gleiche chemische Eigenschaften. Ihre Atommassenzahlen sind jedoch
unterschiedlich. Isotope stehen daher an derselben Stelle im Periodensystem der Elemente.
Viele
Elemente sind Mischungen verschiedener Isotopenarten (Bsp.: Kohlenstoff
mit dem bekanntesten Isotop 14C, 14 = Nukleonenzahl (Kernbausteine) = annähernd Atommassenzahl). Diese Elemente sind
als Mischelemente ein Isotopengemisch. Reinelemente wie Fluor,
Natrium bestehen aus nur einer Atomart. Sie enthalten keine Isotope |
|
nach
oben
|
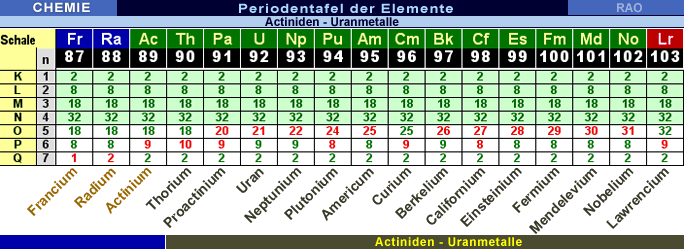
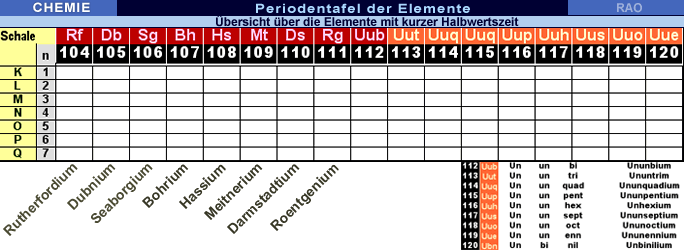
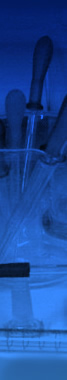
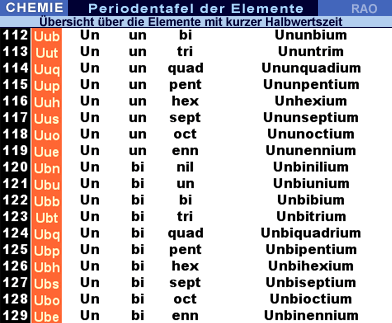
Periodensystem
der Elemente: Schwerelemente
|
 |
nach
oben
nach
oben
|
Links
|
 |
 |
 |
Externe Links |
|